Những quy định mới mà chính quyền Trump áp đặt lên vắc-xin COVID-19 của Novavax đang gây ra sự bất ổn cho việc cập nhật các loại vắc-xin khác.
Novavax cho biết FDA yêu cầu họ thực hiện một thử nghiệm lâm sàng mới sau khi cơ quan này cấp phép đầy đủ cho vắc-xin của họ. Công ty cho biết họ đã phản hồi và tin rằng vắc-xin của họ vẫn “có thể được phê duyệt”.
Ủy viên FDA Marty Makary cho rằng có thể cần một thử nghiệm mới trước khi vắc-xin được cập nhật chủng hàng năm, điều này khó có thể thực hiện được trước mùa thu. Điều này làm dấy lên câu hỏi liệu các loại vắc-xin khác có bị ảnh hưởng hay không.
Tiến sĩ Jesse Goodman của Đại học Georgetown, cựu lãnh đạo vắc-xin của FDA, cho biết: “Tôi không nghĩ rằng vì có sự thay đổi chủng mà đây là một sản phẩm mới”. Nếu đó là chính sách mới, “bạn sẽ luôn phải thực hiện các thử nghiệm lâm sàng và bạn sẽ không bao giờ có một loại vắc-xin nào được cập nhật”.
Động thái bất thường tại FDA diễn ra ngay sau khi lãnh đạo vắc-xin lâu năm của cơ quan này bị buộc phải rời đi vì bất đồng với cấp trên của Makary, Bộ trưởng Y tế Robert F. Kennedy Jr.
Kennedy đã giành được sự xác nhận của Thượng viện cho công việc của mình, một phần bằng cách hứa sẽ không thay đổi lịch tiêm chủng của quốc gia. Kể từ khi nhậm chức, ông đã hứa sẽ “điều tra” các mũi tiêm cho trẻ em, hủy bỏ các cuộc họp của các cố vấn vắc-xin chuyên gia và chỉ đạo các quan chức xem xét lại các mối liên hệ giữa vắc-xin và chứng tự kỷ, một mối liên hệ đã bị bác bỏ từ lâu.
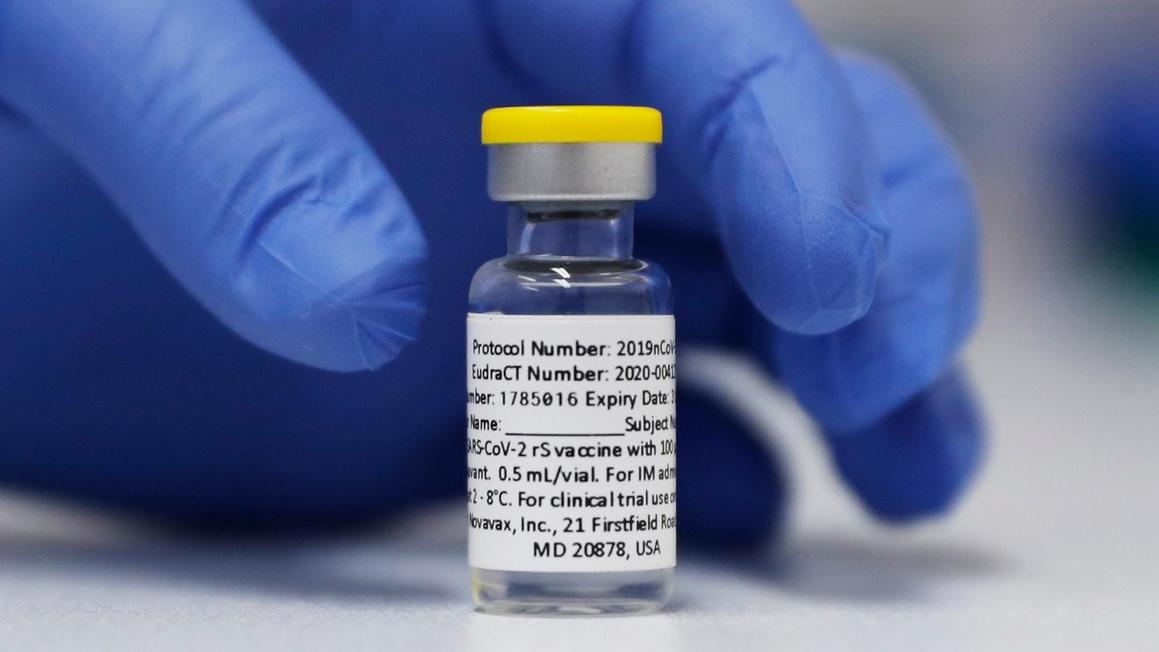
Vắc-xin Novavax, ban đầu cho thấy hiệu quả trong một thử nghiệm lâm sàng gần 30.000 người, vẫn đang được bán theo ủy quyền sử dụng khẩn cấp ở Hoa Kỳ. Hai lựa chọn khác của quốc gia, vắc-xin mRNA do Pfizer và Moderna sản xuất, đã được FDA phê duyệt đầy đủ cho một số nhóm tuổi nhất định.
Vì coronavirus liên tục đột biến, các nhà sản xuất tuân theo hướng dẫn từ FDA để thực hiện một thay đổi mỗi năm đối với công thức của họ — chủng nào cần nhắm mục tiêu — giống như vắc-xin cúm.
FDA đã đi đúng hướng để cấp phép đầy đủ cho Novavax vào ngày 1 tháng 4, theo hai người có kiến thức trực tiếp về tình hình, những người đã nói với điều kiện giấu tên để thảo luận về các vấn đề bí mật của cơ quan. Nhưng những người được Trump bổ nhiệm đã chỉ đạo các nhà khoa học của FDA tạm dừng quyết định của họ, theo một trong những người này. Kể từ động thái rất bất thường đó, Novavax và cơ quan này đã thảo luận về các yêu cầu bổ sung để phê duyệt.
Trong một bài đăng trên mạng xã hội, Makary gọi vắc-xin Novavax là “một sản phẩm mới”, có lẽ vì nó đã được cập nhật để phù hợp với chủng coronavirus phổ biến của năm ngoái.
“Sản phẩm mới đòi hỏi các nghiên cứu lâm sàng mới,” Makary nói thêm.
Một phát ngôn viên của chính quyền đã không trả lời các câu hỏi cụ thể về Pfizer và Moderna, nhưng gợi ý rằng tất cả các loại vắc-xin COVID-19 có thể phải đối mặt với các yêu cầu nghiêm ngặt hơn.
“Đã nhiều năm kể từ khi COVID gây ra mối đe dọa như trước đây và sự khẩn cấp phải đẩy nhanh việc phê duyệt các loại vắc-xin tăng cường mà không có sự giám sát thông thường không còn tồn tại,” Andrew Nixon, phát ngôn viên của Bộ Y tế và Dịch vụ Nhân sinh, cho biết trong một tuyên bố.
FDA đã đối xử với các bản cập nhật chủng COVID-19 hàng năm giống như cách họ đã làm trong nhiều thập kỷ với vắc-xin cúm — không phải là sản phẩm mới, mà là sản phẩm hiện có chỉ được điều chỉnh để bảo vệ chống lại các chủng mới nhất, Tiến sĩ Paul Offit, một chuyên gia về vắc-xin tại Bệnh viện Nhi đồng Philadelphia, cho biết.
Offit cho biết các công ty vẫn phải thực hiện các xét nghiệm trên một số lượng nhỏ người cho thấy các loại vắc-xin cập nhật này tạo ra mức độ kháng thể chống lại vi-rút được biết là có khả năng bảo vệ và chúng được theo dõi chặt chẽ về độ an toàn.
Nixon, phát ngôn viên của HHS, gợi ý rằng chính sách này có thể không áp dụng cho vắc-xin cúm, “vốn đã được thử nghiệm và kiểm tra trong hơn 80 năm”.
Theo luật liên bang, FDA được yêu cầu tuân theo các quy trình đã được thiết lập khi đưa ra các yêu cầu cho các nhà sản xuất thuốc để phê duyệt. Nếu cơ quan này bỏ qua một số bước nhất định hoặc áp đặt các yêu cầu bổ sung vì lý do chính trị, các chuyên gia cho biết, các nhà sản xuất thuốc — hoặc thậm chí cả bệnh nhân, chẳng hạn như những người thích vắc-xin Novavax hơn các đối thủ cạnh tranh vì dị ứng hoặc một số lý do khác — có thể kiện.
Ngoài các thử nghiệm lâm sàng lớn được thực hiện trước khi cả ba loại vắc-xin COVID-19 được phép sử dụng, còn có dữ liệu về việc sử dụng trong thế giới thực, cựu Bộ trưởng Y tế Xavier Becerra, người giám sát chính sách vắc-xin COVID-19 trong chính quyền Biden, cho biết.
“Tại thời điểm tôi rời đi, chúng tôi đã đưa khoảng 700 triệu vắc-xin COVID vào tay người Mỹ,” ông nói. “Đó là một thử nghiệm lâm sàng có quy mô khá lớn.”
Theo tin từ AP News.